Introduzione
Secondo la definizione della IASP (International Association for the Study of Pain – 1986) e dell’Organizzazione mondiale della sanità, il dolore «è un’esperienza sensoriale ed emozionale spiacevole associata a danno tissutale, in atto o potenziale, o descritta in termini di danno» (1).
Esso non può essere descritto esclusivamente come un fenomeno sensoriale, bensì deve essere visto come la composizione di una parte percettiva (la nocicezione) che costituisce la modalità sensoriale che permette la ricezione e il trasporto al sistema nervoso centrale di stimoli potenzialmente lesivi per l’organismo e una parte esperienziale (quindi del tutto privata, la vera e propria esperienza del dolore) che è lo stato psichico collegato alla percezione di una sensazione spiacevole (2,3).
Una sedazione troppo profonda potrebbe mascherare una non corretta o superficiale gestione del dolore. Al tempo stesso una sedazione insufficiente aumenta il rischio di auto-estubazione, problematiche cardiovascolari e danni fisici (4). Il livello di sedazione dovrebbe variare a seconda delle esigenze di ogni paziente senza sottovalutare algie di varia eziologia, e stati di malattia eventualmente preesistenti (5). Le cause della presenza di dolore in pazienti ricoverati in terapia intensiva sono numerose: la presenza di patologie concomitanti, le procedure invasive, la ventilazione meccanica, la presenza del tubo endotracheale, le ferite chirurgiche, le procedure infermieristiche possono essere stimoli che, da soli o presenti contemporaneamente, possono causare dolore (4). Da un recente studio europeo condotto in collaborazione tra l’Università di Göteborg e l’Università di Boras in Svezia è emerso come anche solo il rumore in rianimazione sia fonte di stress per i pazienti (6). I degenti ricoverati nelle terapie intensive, infatti, sono soggetti a livelli di rumore di oltre 20 decibel più alti di quelli raccomandati dalla Organizzazione Mondiale della Sanità per questi reparti. Poiché quindi il dolore è un problema rilevante e diffuso in terapia intensiva, la sua gestione risulta prioritaria per una completa cura del paziente e il primo passo è una sua corretta valutazione. Già nei primi anni Novanta, precisamente nel 1992, l’Agency for Health Care Policy and Research (AHCPR) ha pubblicato le prime linee guida, aggiornate poi nel 2014 (7), per l’accertamento del dolore, raccomandando il monitoraggio di parametri fisiologici e la valutazione delle risposte comportamentali agli stimoli dolorosi. Le scale quantitative VAS (scala analogica visiva), NRS (scala numerica visiva), VRS (scala di valutazione verbale), che sono forse le più comuni scale soggettive (Figura 1), spesso non sono di grande utilità nella cura del paziente critico. La rilevazione del dolore nelle terapie intensive non è sempre possibile, principalmente perché i pazienti sono spesso in uno stato di incoscienza, farmacologico e non. Ciò non toglie che un’adeguata analgesia rimanga comunque fondamentale. Il dolore non controllato sviluppa infatti tachicardia, abbassamento delle difese immunitarie, aumento della produzione di catecolamine e maggior consumo di ossigeno (8-10). Già dai primi anni 2000 sono stati pubblicati diversi lavori sulla valutazione del dolore in pazienti intubati, sedati o non in grado di comunicare. Studi di follow-up su pazienti dimessi dalle terapie intensive tramite la Icu Memory Tool (11) hanno evidenziato che spesso gli intervistati ricordavano di avere avuto molto dolore durante il ricovero. Dalla revisione della letteratura sono emersi due strumenti validati per l’accertamento in terapia ntensiva in soggetti ventilati meccanicamente: la Behavioral Pain Scale (12) (BPS) e la Critical-Care Pain Ob-servation Tool (13-17) (C-CPOT) (Figura 2). La scala BPS è costituita solo da 3 item: espressione facciale, movimenti degli arti e compliance con la ventilazione meccanica. La C-CPOT prevede invece 4 item di cui l’item 3 può variare secondo il contesto clinico: espressione facciale, movimenti del corpo, compliance al ventilatore o vocalizzazione, tensione muscolare. Questa scala può essere di grande utilità nel valutare i pazienti che non sono in grado di comunicare con il personale sanitario anche se non intubati. La C-CPOT è stata validata in Italia da F. Stefani et al. nel 2011 (18), e la BPS è stata validata in Italia da L. Falbo et al. nel 2013 (19). Nell’ipotesi che nella realtà delle terapie intensive italiane l’utilizzo di scale di valutazione del dolore adeguate ai pazienti critici sia scarsamente diffuso, abbiamo effettuato uno studio esplorativo sottoponendo una survey alle rianimazioni aderenti al Gruppo Italiano per la Valutazione degli Interventi in Terapia Intensiva (GiViTi), riguardante il metodo utilizzato abitualmente per valutare il dolore nei pazienti ricoverati.
Materiali e metodi
Per effettuare questo studio abbiamo condotto un’indagine osservazionale trasversale in un periodo di tempo compreso tra il 10 marzo e il 30 maggio 2015. Per la raccolta dei dati è stato utilizzato un questionario volto a esaminare l’utilizzo di strumenti e metodi di rilevazione del dolore in terapia intensiva. Previo consenso del comitato tecnico scientifico e del Presidente dell’associazione, abbiamo contattato via e-mail tutte le terapie intensive italiane aderenti al GiViTi. Il questionario è stato diffuso come allegato a un’e-mail di presentazione, dove veniva reso esplicito lo scopo dell’indagine. Non è stato necessario contattare il Comitato Etico di ogni ospedale coinvolto in quanto non si tratta di uno studio in cui vengano arruolati pazienti, non vi è carattere sperimentale e non vengono raccolti dati sensibili. Tutte le informazioni sono state immagazzinate in forma anonima e le varie terapie intensive sono state identificate con un numero progressivo in cifra araba da 1 a 173. I dati raccolti sono stati immagazzinati in un database il cui accesso è regolamentato da normative di sicurezza in materia di privacy (D.Lgs. 196/2003).
Nel questionario veniva chiesto di segnalare i dati descrittivi della struttura così come gli strumenti utilizzati per valutare il dolore. Nello specifico di indicare:
- localizzazione geografica della terapia Intensiva (Nord, Centro, Sud);
- il tipo di Rianimazione (polivalente o specialistica);
- i pazienti assistiti (adulti, adulti/pediatrici, pediatrici);
- quale tra le seguenti scale veniva utilizzata per la valutazione del dolore, (erano ammesse anche più di una risposta): BPS (Behavioral Pain Scale), C-CPOT (Critical-Care Pain Ob-servation Tool), VAS (visual analogue scale), VRS (scala di valutazione verbale), NRS (numerical rating scale), CHEOPS (Children’s Hospital of Eastern Ontario PainScale), PRS (Happy Face Pain Rating Scale), NVPS (Non Verbal Pain Sale).
Alla fine del questionario veniva chiesto di motivare la scelta di una scala rispetto alle altre.
Le terapie intensive coinvolte sono state suddivise in base all’utilizzo di scale di valutazione del dolore ritenute adeguate all’ambito intensivo (BPS e C-CPOT) o inadeguate (tutte le altre).
I dati raccolti sono stati inseriti in un foglio di calcolo Microsoft ExcelR 2010.
Analisi statistica
L’analisi dei dati è stata effettuata con il software SPSS 17.0 (SPSS inc., Chicago, IL). L’associazione tra adeguatezza nella valutazione del dolore e variabili qualitative (tipo di rianimazione, tipo di pazienti assistiti) è stata valutata mediante test chi-quadrato; per la variabile localizzazione geografica è stato utilizzato un test statistico per variabili non parametrici (Mann-Whitney).
Risultati
Hanno partecipato alla survey 173 unità operative, su un totale di 515 unità di terapia intensiva contattate. I dati pervenuti riguardano rianimazioni polivalenti (78,6%) e specialistiche (21,4%). Per quanto riguarda la distribuzione geografica delle rianimazioni che hanno risposto, la maggior parte dei questionari compilati è arrivata dal nord Italia (p<0.001, Tabella 1).
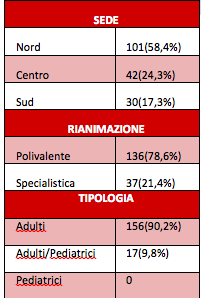
I dati GiViTi sono pervenuti da 15 regioni d’Italia (Tabella 2), e una certa quota di terapie intensive ha dichiarato che utilizza più di una scala per la valutazione del dolore (33%). La scala più diffusa è risultato il gruppo NRS/VAS (55%). La diffusione di scale del dolore definite come adeguate (BPS e C-CPOT) per la valutazione del dolore nel paziente intubato è risultata del 24% (BPS 14% e C-CPOT 10% dei rispondenti).
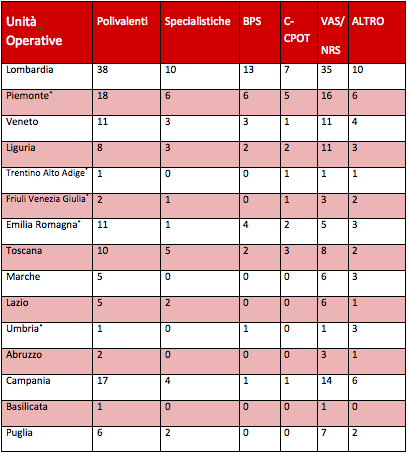
La diffusione di queste scale tende a diminuire da nord a sud (p<0.001) e non è risultata associata al tipo di rianimazione contattata (polivalente vs specialistica, p=0.826, Tabella 3).
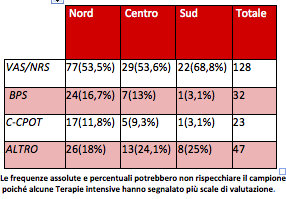
L’associazione VAS/NRS e BPS o VAS/NRS e C-CPOT è stata riscontrata in circa il 50% delle terapie intensive che hanno dichiarato l’utilizzo di più scale, corrispondente al 17% del totale.
Il 21% delle terapie intensive contattate utilizza scale non oggettive diverse, non utilizza scale o si basa su i parametri vitali. Tra queste in particolare 6 Rianimazioni accertano il dolore in seguito alla modificazione di alcuni parametri vitali, mentre in un caso il dolore non viene mai valutato. Una Terapia Intensiva utilizza altre scale (scala Flacc) oltre a quelle da noi illustrate nella survey.
Tra le motivazioni citate all’interno del questionario sull’utilizzo della scala VAS vi è la condivisione da parte di tutto il personale, la semplicità d’utilizzo e la direttiva aziendale.
Discussione
In questo studio abbiamo riscontrato che la diffusione di scale di valutazione giudicate idonee alla valutazione del dolore in pazienti intubati (BPS e C-CPOT) è ad oggi poco diffusa tra le terapie intensive che hanno risposto alla nostra survey.
Le linee guida sul trattamento del dolore nei traumatizzati sottolineano come questo sintomo sia relegato al rango di “sintomo minore” e confermano l’opportunità della adozione di scale e strumenti di misura soggettiva del dolore percepito dal paziente, al fine di trattarlo in modo più adeguato. Abbiamo a priori definito adeguato l’utilizzo delle scale BPS e C-CPOT per accertare il dolore in pazienti sottoposti a ventilazione meccanica sulla base di quanto riportato dalla letteratura /12-17) (C-CPOT). Le due scale sono state validate nel 2011 (C-CPOT) e 2013 (BPS), tradotte e poi ritradotte nella lingua originale in modo da apportare un’equivalenza linguistica e culturale tra la scala originale e quella italiana. Nei pazienti ventilati meccanicamente, la BPS, o la C-CPOT, può essere strumenti utili insieme all’esperienza clinica dell’infermiere e all’osservazione dei parametri vitali. Le caratteristiche essenziali di una scala vengono mantenute da entrambe, sia come semplicità che come rapidità di utilizzo. La diffusione di queste scale nel campione analizzato è stata inferiore al 25%, particolarmente carente al Centro-Sud. Tuttavia, il dato di distribuzione geografica potrebbe essere influenzato da una non omogenea distribuzione delle terapie intensive rispondenti.
Le scale VAS e NRS sono uno strumento di misurazione soggettiva del dolore che è utile in terapia intensiva solo quando il contesto clinico lo permette, vale a dire quando il paziente è contattabile e in grado di esprimersi. Queste condizioni si verificano in una quota di pazienti (per esempio il post-operato estubato), ma possono non verificarsi anche per molti giorni di seguito in pazienti critici complessi. Ciononostante, il gruppo VAS/NRS nel contesto italiano rappresenta attualmente il metodo più diffuso (nel 55% dei casi) per la misurazione del dolore. Abbiamo deciso di raggruppare le scale VAS e NRS poiché si basano sostanzialmente sugli stessi elementi e riteniamo che sia diffusa la possibilità di confonderle tra loro nel gergo comune.
Anche le scale che abbiamo a priori definito adeguate hanno dei limiti. In uno studio di Pudas-Tahka et al.(20) si evidenzia che la BPS può trarre in inganno l’operatore sanitario, che talvolta può enfatizzare la sintomatologia dando un risultato operatore-dipendente in seguito alla valutazione e osservazione dei comportamenti. Infine, alcuni aspetti come l’ipossia, l’agitazione, il disagio, possono essere riscontrati anche in pazienti che non hanno dolore. È pertanto fondamentale considerare questi fattori come probabili fattori confondenti. La sola osservazione dei comportamenti non è il modo migliore per rilevare il dolore. La valutazione dei parametri emodinamici, quali l’aumento della frequenza cardiaca, l’incremento della pressione arteriosa e l’aumento della frequenza respiratoria, associati talvolta a lacrimazione e dilatazione pupillare, viene vista come utile metodo di accertamento in 6 rianimazioni, durante le attività di nursing o le procedure invasive, quali ad esempio il posizionamento del sondino nasogastrico, cateterismo vescicale, puntura radiale, rimozione dei drenaggi, palpazione addominale, mobilizzazione. All’interno di un’Unità di Neurorianimazione, il dolore non viene valutato in nessun modo. Se ciò è corretto o meno, in questo caso dipende dalla diagnosi di ogni singolo paziente all’interno del proprio reparto.
Una quota bassa di terapie intensive utilizza più modalità di valutazione del dolore; l’utilizzo di scale adeguate in base allo stato clinico del paziente (una scala per pazienti in ventilazione meccanica e una per pazienti in grado di esprimersi) è stato riscontrato in un numero limitato di casi (17%). Riteniamo che la situazione ideale sia l’essere in grado di utilizzare la scala più adeguata alle condizioni del paziente, il che potrebbe anche implicare l’utilizzo di una scala nei primi giorni di ricovero e di una scala differente al variare del quadro clinico. L’utilizzo di almeno due scale non risolve del tutto la problematica della valutazione dolore (sarebbe interessante conoscere nelle rianimazioni dove si utilizza doppia scala, BPS e VAS/NRS, come viene valutato il paziente non ventilato meccanicamente e non orientato spazio-tempo), ma rappresenta certamente un significativo miglioramento nella cura dei pazienti ricoverati in terapia intensiva.
Conclusioni
Lo scopo dell’indagine è stato esplorare un campione rappresentativo di terapie intensive italiane al fine di evidenziare all’interno di esse i metodi o gli strumenti utilizzati per la rilevazione del dolore. Il risultato ci porta a notare come a distanza di oltre 10 anni dalla validazione di scale adeguate alla valutazione del dolore nel paziente critico (BPS e C-CPOT), la maggioranza del nostro campione non ne fa utilizzo e quindi non possiede specifici strumenti per la valutazione nei pazienti sottoposti a ventilazione meccanica o sedati.
Ringraziamenti
Gli autori ringraziano C. Ripamonti, Coordinatore dell’U.O. della Rianimazione A. Manzoni di Lecco e l’associazione GiViTi.
Bibliografia
1. Merskey H, Bogduk N. Classification of chronic pain description of chronic pain syndrome of pain terms. Second Edition. Harold Merksey ed., 1994.
2. Merskey H. Development of a universal language of pain syndromes. In: J.J. Bonica, U. Lindblom and A. Iggo (Eds.), Proceedings of the Third World Congress on Pain. Advances in Pain Research and Therapy, Vol. 5. Raven Press: New York; 1983: 37-52.
3. Mannion RJ, Woolf CJ. Pain mechanisms and management: a central perspective. Clin J Pain. 2000; 16(3 Suppl): S144-56.
4. Bambi S, Lumini E, Lucchini A, Rasero L. Unplanned extubations in adult intensive care units: an update Assist Inferm Ric. 2015; 34(1): 21-9. doi: 10.1702/1812.19748.
5. Grap MJ, Munro CL, Wetzel PA, Best AM, Ketchum JM, Hamilton VA, Arief NY, Pickler R, Sessler CN. Sedation in adults receiving mechanical ventilation: physiological and comfort outcomes. Am J Crit Care 2012; 21(3):e53-63; quiz e64. doi: 10.4037/ajcc2012301.
6. Johansson L, Bergbom I, Waye KP, Ryherd E, Lindahl B. The sound environment in an ICU patient room–a content analysis of sound levels and patient experiences. Intensive Crit Care Nurs 2012; 28(5): 269-79. doi: 10.1016/j.iccn.2012.03.004.
7. Clinical Guidelines and Recommendations. Agency for Healthcare Research and Quality. Rockville MD. November 2014.
8. Hughes CG, McGrane S, Pandharipande PP. Sedation in the intensive care setting. Clin Pharmacol. 2012; 4: 53-63. doi: 10.2147/CPAA.S26582.
9. Acute Pain Management Guideline Panel. Acute Pain Management Operative or Medical Procedures and Trauma. Clinical Practice Guideline No.1. Rockville, Md; Us Dept of Health and Human Services, Agency for Health Care Policy and Research, 1992. Publication 92-0032.
10. Berben SA, Kemps HH, van Grunsven PM, Mintjes-de Groot JA, van Dongen R, Schoonhoven L. Guideline “Pain management for trauma patients in the chain of emergency care”. Ned Tijdschr Geneeskd 2011; 155: A3100, PMID 21771359.
11. Jones C, Humphris GM. Preliminary validation of the ICUM tool: a tool for assessing memory of the intensive care experience. Clinical Intensive Care 2000; 11(5):251-255. DOI: 10.1080/714028717.
12. Payen JF, Bru O, Bosson JL, Lagrasta A, Novel E, Deschaux I, Lavagne P, Jacquot C. Assessing pain in critically ill sedated patients by using a behavioral pain scale. Crit Care Med 2001; 29(12): 2258-63.
13. Gèlinas C, Fortier M, Viens C, Fillion L and Puntillo KA. Pain assessment and management in critically ill intubated patients: a retrospective study. American Journal of Critical Care 2004; 13: 126-136.
14. Gélinas C, Arbour C, Michaud C, Vaillant F, Desjardins S. Implementation of the critical-care pain observation tool on pain assessment/management nursing practices in an intensive care unit with nonverbal critically ill adults: a before and after study. International Journal of Nursing Studies, 2011; 48: 1495-1504.
15. Gélinas C, Arbour C. Behavioral and physiologic indicators during a nociceptive procedures in conscious and unconscious mechanically ventilated adults: Similar or different? Journal of Critical Care 2009; 24: 628.e7–628.e17.
16. Gélinas C, Fillion L, Puntillo KA, Viens C, Fortier M. Validation of the Critical-Care Pain Observation Tool in adult patients. American Journal of Critical Care 2006; 15: 420-427.
17. Gélinas C, Johnston C. Pain assessment in the critically ill ventilated adult: validation of the critical-care pain observation tool and physiologic indicators. Clinical Journal of Pain 2007; 23: 497-505.
18. Stefani F, Nardon G, Bonato R, Modenese A, Novello C, Ferrari R. The validation of C-POT Critical-Care Pain Observation Tool scale: a tool for assessing pain in intensive care patients. Assist Inferm Ric 2011; 30(3): 135-43. doi: 10.1702/970.10587.
19. Falbo L, Terzoni S, Destrebecq A,Bonetti L. Traduzione e validazione in italiano della Behavioral Pain Scale (BPS) per la valutazione del dolore in pazienti incoscienti e sedati. Scenario 2013; 30(4): 18-23.
20. Putas-Tahka SM, Axelin A, Aantaa R, Lund V, Salantera S. Pain assessment tools for unconscious or sedated intensive care patients: a systematic review. J Adv Nurs 2009; 65: 946-956.
