Il CPP viene descritto come una malattia debilitante per molte donne, che non riconosce una unica eziologia, ma che può essere correlata a patologie urogenitali come l’endometriosi, la dispaurenia, i leiomiomi, l’adenomiosi, oppure legato a malattie gastrointestinali o scheletriche (3-5). Alcune ricerche hanno evidenziato un legame con la cistite interstiziale (IC) (5,6).
Dal punto di vista epidemiologico la sua prevalenza varia da Paese a Paese, in virtù della multi-eziologia associata, della distribuzione per fasce di età e della durata della sintomatologia dolorosa. I range variano da 3,7% a 4,1% nei Paesi dell’America Latina (7), al 15% negli USA (8). In Italia è stata stimata intorno al 13,8% (9). Una recente revisione quantifica la prevalenza tra il 5,7% e il 26,6% (10).
Il CPP in relazione all’impatto che può avere sullo svolgimento delle attività di vita quotidina ed al suo potenziale effetto invalidante, può divenire causa di perdita di lavoro, e può associarsi a depressione, ansia e alterazione del ritmo sonno-riposo (11-13).
La sintomatologia dolorosa può originarsi sia dagli stessi organi interni della pelvi, come l’utero e la vescica, sia da quelli ad essi correlati, come la parete addominale e pelvica (14), che possono rendere difficoltoso l’inquadramento diagnostico.
Sono stati sviluppati diversi protocolli in merito alla gestione e trattamento del CPP (15-17). Trattandosi di una condizione clinica ad eziologia multipla, si ritiene necessario un approccio terapeutico che tenga conto della multidisciplinarietà (18,19), in cui possono essere attuati diversi trattamenti, quali quelli farmacologici, chirurgici, ormonali, fisici e in alcuni casi anche quelli complementari (20).
In virtù della multieziologia del CPP e della complessità dei trattamenti potenzialmente efficaci, si rende utile identificare e descrivere il potenziale panorama dell’offerta terapeutica.
Lo scopo di questa revisione è quello di descrivere gli approcci in letteratura utili a gestire il CPP.
Lo studio di revisione si è focalizzato sulla popolazione di donne in età fertile, con esclusione dei soggetti adolescenti, gravide, o che focalizzassero la loro attenzione al dolore correlato alla dismenorrea e alla dispaurenia.La query di ricerca è stata formulata seguendo la metodologia PICO:


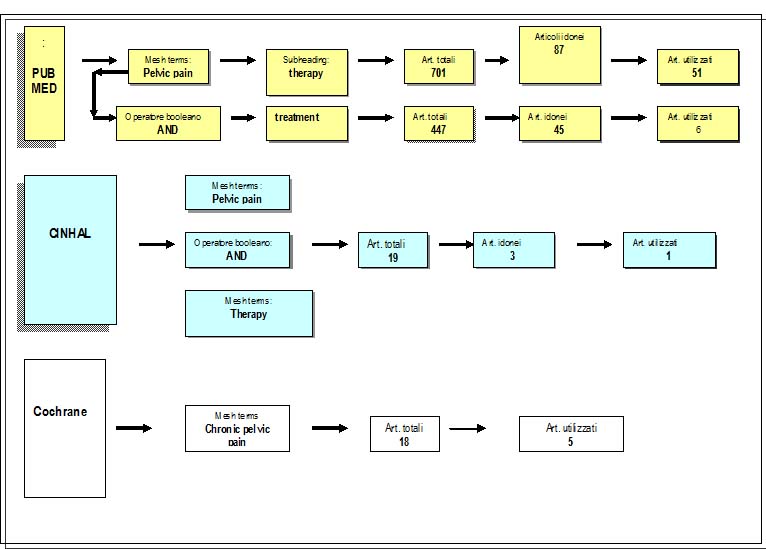
Gli articoli e le rassegne inclusi sono elencati nelle tabelle 3 e 4.
Tabella 3 – Articoli inclusi
|
Anno |
Autore |
Titolo |
Tipo di studio |
|
risultati |
|
2011 Pub med |
Corbellis et al |
Efficacia dell’associazione micronizzato N – Palmitoylethanolamide (PEA)-transpolydatin nel trattamento del dolore pelvico cronico da endometriosi dopo una valutazione laparoscopica: uno studio pilota. |
Randomized controlled trial (Rct) |
61 donne randomizzate in tre gruppi uno in terapia con la PEA e la Polidatina (gruppo A), l’altro con il placebo ( gruppo B) e il terzo con una COX2 il celecoxib (gruppo C). |
Riduzione del dolore pelvico statisticamente significativo nel gruppo A rispetto al B (p<0.01); diminuzione del dolore rispetto al gruppo in trattamento con il Celecoxib, risulta minore nel confronto con il gruppo PEA.
|
|
2004 Pub med |
Ailawandi et al |
Trattamento dell’endometriosi e dolore pelvico cronico con letrozolo e noretindrone acetato: uno studio pilota. |
Rct |
Studio sul ruolo di un inibitore dell’aromatasi sull’endometrio associato a norentindrone acetato in 10 pazienti. |
L’associazione dell’inibitore e la terapia di supporto sono efficaci nel controllo del dolore. |
|
2011 Pub med |
Guzick et al |
Trial clinico randomizzato sulla leuprolide versus la somministrazione continua dei contraccetivi orali nel trattamento dell’endometriosi associata al dolore pelvico. |
Rct |
47 pazienti randomizzati per comparare l’efficacia del leuprolide vs contraccettivi orali. |
Ambedue i trattamenti risultatano essere efficaci sul dolore pelvico cronico da endometriosi. |
|
2011 Pub med |
Bayoglu Tekin et al |
Trattamento medico postoperatorio del dolore pelvico cronico legato alla grave endometriosi: sistema intrauterino a rilascio a base di levononogestrel Sistema intrauterino a rilascio versus sistema a rilascio di GnRH analoghi. |
Rct |
40 donne con endometriosi randomizzate tra dispositivi intrauterini (LNG-IUS) e depot con GnRH analoghi. |
Ambedue le metodiche risultano efficaci senza differenze statisticamente significative nel controllo del dolore. |
|
2006 Pub med |
Razzi et al |
L’uso di preparati a base di solo progestinici contenente desogestrel nel trattamento del dolore pelvico ricorrente dopo chirurgia conservativa per endometriosi. |
Rct |
40 donne dopo trattamento chirurgico conservativo vengono randomizzate e confrontate con trattamento a base di progestinici o estroprogestinici. |
Nessuna differenza statisticamente significativa per il dolore pelvico cronico.
|
|
2009 Pub med |
Harada et al |
Il Dienogest è efficace come il buserelin acetato somministrato per via intranasale per il sollievo nei sintomi del dolore associato all’endometriosi – studio clinico randomizzato controllato multicentrico. |
Rct multicentrico |
261 donne con endometriosi vengono confrontate tra uno spray nasale a base di GnRH analoghi e un progestinico. |
Nessuna differenza statisticamente significativa tra i due trattamenti nella sintomatologia dolorosa. |
|
2010 Pub med |
Strowitzki et al |
L’impiego del Dienogest nel trattamento dell’endometriosi associata al dolore pelvico: uno studio controllato di 12 settimane randomizzato doppio cieco. |
Rct multicentrico |
198 donne con endometriosi vengono confrontate tra dienogest e placebo. Il trattamento dura 12 settimane. |
Differenza statisticamente significativa nel dolore con VAS scale ( 12.3 mm in favore del dienogest p<0.0001). |
|
2011 Pub med |
Kitawaki et al |
Terapia di mantenimento con Dienogest che fa seguito alla somministrazione di GnRH agonisti per endometriosi associato a dolore pelvico. |
Rct |
78 donne affette da endometriosi che vengono randomizzate in due gruppi: gruppo G a cui viene somministrato dienogest dopo 4-6 mesi di trattamento con GnRH analoghi; gruppo D a cui viene somministrato solo dienogest. |
Differenza statisticamente significativa nel gruppo G (p<0.01) nei punteggi ottenuti con la VAS scale rispetto alle rilevazioni di partenza. |
|
2011 Pub med |
Abushahin et al |
Gli inibitori dell’aromatasi nella terapia dell’endometriosi refrattaria correlata al dolore pelvico cronico. |
Osservazionale retrospettivo |
60 pazienti vengono valuate dopo aver assunto letrozole (inibitore dell’aromatasi) per 180 gg. |
Si è osservata una riduzione del dolore significativa nelle donne trattate con letrozole (media score pain iniziale 7 vs 1.5 finale). |
|
2009 Pub med |
Verma et al |
Successo terapeutico nell’endometriosi refrattaria correlata al dolore pelvico cronico con gli inibitori dell’aromatasi nelle donne in premenopausa. |
Osservazionale prospettico |
4 pazienti refrattari ad altri trattamenti per l’endometriosi ed il CPP associato sono state valutate dopo trattamento con (AI) associato a trattamento con calcio e vit.D per 6 mesi. |
Si è osservato un rimarchevole diminuzione del punteggio medio del dolore (9 vs 4.5). |
|
2004 Pub med |
Corbellis et al |
Il trattamento con COX-“ inibitori è efficace nella gestione del dolore correlato all’endometriosi |
Rct |
28 donne sono state suddivise in due gruppi in maniera random e sono state sottoposte a trattamento per 6 mesi rispettivamente con COX-2 o placebo. |
Dopo 6 mesi di trattamento sono state osservate delle differenze statisticamente significative nei pazienti trattati con COX-2 (p<0.0001) nella valutazione del dolore. |
|
2008 Pub Med |
Stratton et al |
Il ritorno del dolore pelvico cronico da endometriosi dopo il trattamento con Raloxifenen
|
Rct |
93 donne vengono randomizzate tra trattamento con Raloxifene e gruppo placebon |
Ricomparsa precoce del dolore pelvico (P=0.03) nel gruppo trattamento che costringe le donne a nuovo intervento. |
|
2011 Pub med |
Roth et al |
Fattori psicologici nel dolore pelvico cronico da endometriosi: uno studio comparativo |
Osservazionale |
Oggetto dello studio donne affette da CPP divise in tre gruppi eziologici: endometriosi, dolore miofasciale e dolore pelvico da ederenze. Viene indagato se nell’endometriosi esistono delle variabili psicologiche associate rispetto alle altre forme di CPP. |
lo studio non ha messo in luce differenze statisticamente significative riguardo componenti psicologiche associate all’endometriosi |
|
2009 Pub med |
Montenegro et al |
I cambiamenti posturali nelle donne con dolore pelvico cronico: uno studio caso controllo. |
Studio caso-controllo |
108 donne affette da CPP vengono confrontate con 48 donne sane relativamente alla postura. |
Differenze significative posturali nelle donne con CPP (p<0.01) nel segmento superiore del corpo relativamente alla scapola e alla zone cervicale |
|
2011 Pub med |
Neville et al |
Un report preliminare delle disfunzioni muscoloscheletriche nelle donne con dolore pelvico cronico: uno studio mascherato dei punteggi assegnati all’esame fisico. |
Rct |
48 donne di cui 19 affette da CPP e 29 sane vengono valutate in maniera random relativamente a 9 esami fisici. |
Risultati statisticamente significativi relativi al dolore 2.83 sani vs 5.32 CPP inoltre è stato rilevato nelle donne esaminate affette da CPP un valore medio di disfunzioni muscolo scheletriche più alto nelle donne con CPP |
|
2011 Pub med |
Kaercher et al |
Baropodometria sulle donne che soffrono di dolore cronico pelvico uno studio cross- sectional. |
Studio osservazionale |
32 donne con CPP e 30 donne gruppo di controllo su cui viene valutato l’esame baropodometrico. |
Differenza non statisticamente significativa tra i due gruppi(3.82±1.27 kgf/cm2 vs 3.87± 1.21 kgf/ cm2 2.56±1.12 kgf/cm2 vs 2.78±0.95 kgf/cm2 |
|
2011 Pub med |
Paulson et al |
La debolezza della parete anteriore della vagina come sintomo fsico nel dolore pelvico cronico. |
Studio di coorte |
284 pazienti con CPP è stata valutata per debolezza parete muscolare e correlazione tra endometriosi e cistite interstiziale. |
la debolezza della parete muscolare si ritrova nel 93% delle donne affette da endometriosi e nel 96% delle donne affette da cistite interstiziale |
|
2010 Pub med |
Montenegro de Souza et al |
L’importanza della valutazione della debolezza della muscolatura pelvica nelle donne con dolore pelvico cronico. |
Studio osservazionale |
108 donne con CPP e 48 volontarie sono state valutate per la debolezza della parete muscolare. |
Differenza statisticamente signficativa nelle donne con CPP rispetto alle volontarie 58.35vs 4.2% p<0.001 |
|
2012 Pub med |
Cheng et al |
Diagnosi di cistite interstiziale / sindrome della vescica dolorosa in donne con dolore pelvico cronico: uno studio osservazionale prospettico. |
Studio prospettico |
150 donne con IC e sindrome della vescica dolorosa ( bps)vengono studiate in laparoscopia per CPP. |
La prevalenza di IC è pari al 32% ; quella di BPS è del 53% . Nel 60% si rileva oltre a dolori alla vescica l’ endometriosi. Nel 93% le donne hanno sintomi urinari |
|
2004 Pub med |
Chung et al |
La cistite intestiziale nel dolore pelvico cronico persistente post isterectomia. |
rct |
111 donne con CPP dopo isterectomia vengono studiate per IC e vengono create 2 gruppi trattamento e terapia. |
Riduzione del dolore nel gruppo trattamento del 32%. |
|
2012 Pub med |
Fitzgerald et al |
Trial clinico randomizzato multicentrico della terapia miofasciale nelle donne con cistite interstiziale/sindrome della vescica dolorosa e debolezza della parete pelvica. |
Rct multicentrico |
81 donne con CPP da IC e PBS vengono randomizzate tra un gruppo di trattamento con terapia fisica miofascale e terapia con massaggi globali. |
Nel gruppo trattamento si ha una risposta generale nel 60% rispetto al 26 % del gruppo di controllo. |
|
2012 Pub med |
Martinez et al. |
Gestione dei pazienti con dolore pelvico cronico associato ad endometriosi refrattaria a trattamenti convenzionali. |
Studio osservazionale |
44 pazienti refrattari a trattamenti convenzionali per il CPP da endometriosi vengono sottoposti a neuro stimolazione e a blocco delle terminazioni nervose. |
Riduzione del dolore nel 40% dei pazienti trattati con neuromodulazione sia elettrica che chimica. |
|
2013 Pub med |
Nesbitt-Hawes et al |
Miglioramento del dolore pelvico con l’iniezione diella tossina botulinica di tipo A iniezione singola versus iniezione ripetute.
|
Rct |
Confronto nel miglioramento del dolore pelvico tra gruppo con iniezione singola di botox vs iniezioni ripetute. |
In ambedue i trattamenti il dolore si riduce rispetto al valore iniziale, con differenze significative nella dodicesima settimana 45 vs 15 nella singola e 37 vs 12 nella multipla. |
|
2013 Pub med |
Giugliano et al. |
L’uso adiuvante della PEA nel trattamento del dolore da endometriosi. |
Rct |
47 pazienti divisi in due gruppi a seconda del sito endometriosico. Ambedue i gruppi vengono trattati con PEA. |
Diminuzione significativa dell’intensità del dolore in ambedue i gruppi( p<0.0001). |
|
2004 Pub med |
Johnson et al |
Studio randomizzato controllato doppio cieco sull’ablazione del nervo uterino laparoscopico per le donne con dolore pelvico cronico. |
Rct |
123 donne affette sia da endometriosi che da CPP senza evidenza di endometriosi vengono sottoposte a LUNA. |
La tecnica LUNA si è rilevata efficace nella gestione del dolore nelle pazenti affette da dolore pelvico dovuto a dismenorrea (P= 0.045). Non ci sono differenze significative nella gestione del dolore nelle donne affette da endometriosi trattate con LUNA. |
|
2007 Pub med |
Kim et al |
Stimolazione percutanea posteriore del nervo tibiale in pazienti con dolore pelvico cronico: uno studio preliminare. |
Rct (tipo open) |
15 pazienti: 10 donne e 5 uomini vengono sottoposti a stimolazione del nervo tibiale per 12 settimane. |
9 soggetti su 12 hano avuto una riduzione del dolore misurato con la scala di VAS ; 3 invece hanno avuto una riduzione alla VAS tra il 25 e50%. I punteggi medi per il dolore alla VAS sono passati da 8.1 ± 0.2 a 4.5 ± 0.6 dopo 12 settimane di trattamento. |
|
2013 Pub med |
Morelli et al |
Somministrazione postoperatoria di dienogest più estradiolo valerato versus dispositivi intrauterini che rilasciano levonorgestrel per la prevenzione del ritorno del dolore e la ricorrenza della malattia nelle pazienti con endometriosi. |
Rct |
92 pazienti randomizzati per trattamento con dispositivi intrauterini a base di levonorgestrel e il dienogest più estradiolo vengono poi valutati riguardo la ripresa del dolore e la ricorrenza della malattia. |
Il gruppo trattato con dienogest più estradiolo ha avuto una riduzione nel dolore a 12 e 24 mesi rispetto ai pazienti trattati con levonorgestrel, ma senza carattere di significatività statistica. Tuttavia il trattamento con i dispositivi intrauterini si è rilevato più pratico utilizzo rispetto al trattamento con dienogest. |
|
2013 Pub med |
Yong et al. |
Esplorazione inguinale laparoscopica e posizionamento di una rete per il dolore pelvico cronico. |
Studio retrospettivo |
48 pazienti con dolore pelvico cronico localizzato in zona di debolezza inguinale omolaterale vengono indagati per verificare se il posizionamento di una rete riduce la ricomparsa del dolore. |
Moderata riduzione del dolore nei pazienti sottoposti a trattamento chirurgico con posizionamento della rete in pazienti selezionati con zone di debolezza inguinale omolaterale. |
Tabella 4 – Revisioni incluse
|
Anno |
autore |
Titolo |
popolazione |
Tipo di intervento |
Risultati/Outcame |
|
2006 Pub med |
Bordman et al |
Sotto la cintura. Approccio al dolore pelvico |
non dichiarata (nd) |
Terapia medica con FANS, antidepressivi, ormonale, terapia chirurgica: ablazione nervo uterino isterectomia trattamenti locali per zone di trigger point agopuntura trattamenti per IC |
Trattamenti con FANS, ASA, analgesici non narcotici, sono considerati come trattamenti di prima linea (Livello III evidenza) Trattamenti ormonali: contraccettivi orali ( liv. III); progestinici contonui ( Liv.I); GnRH agonisti ( Liv.I) Per dolore refrattario: antidepressivi triciclici ( liv. III); serotonina-norefinefrina inibitori del reuptake ( liv. II); oppioidi ( liv. III) Trattamenti chrurgici: ablazione del nervo come scelta limitata a dolore intermedio (Liv. I); isterectomia che risulta essere meno efficae per donne giovani < 30 aa senza diagnosi precisa ( Liv. II).
|
|
2010 Pub med |
Green et al |
Terapie interventistiche per controllare il dolore pelvico: quali sono le evidenze? |
nd |
Vengono citate le possibili opzioni terapeutiche differenziate in interventi globali e specifici |
· FANS e tramadolo hanno dimostrato efficacia nel controllo del dolore · Antidepressivi sia nel controllo del dolore che come trattamento multimodale · Gabapentin risulta più efficace rispetto l’amitriptilina · Psicoterapia : dimostrata efficace come parte di un approccio multidisciplinare · Neurolisi del plesso ipogastrico e blocco del ganglio · I trattamenti ormonali sono tutti efficaci nel dolore ,ma soo poche le evidenze che un rgime terapeutico sia superiore all’altro · La terapia chirugica laparoscopica con escissioe risulta essere efficace · cistite interstiziale: trattamenti dietetici, terapia medica, trattamenti intravescicali,idrodistenzione, stimolazioni percutanee radice del nervo sacrale, cistectomia parziale.
|
|
2006 pub med |
Ozawa et al |
La gestione del dolore associato a endometriosi: un aggiornamento dei problemi relativi al dolore
|
20-50 donne |
– terapia farmacologica: contraccettivi orali, GnRH analoghi, Danazol – terapia chirurgica: laparoscopica con LUNA
|
Terapia chirurgica : 44.7% delle done manifesta sintomi dopo trattamento Terapia medica: riduce i sintomi ma non esistono evidenze legate ad un uso a lungo termine . |
|
2007 Cochrane |
Farquhar et al |
Danazolo per il dolore pelvico associato a endometriosi |
nd |
Danazolo vs placebo nell’endometriosi anche dopo terapia chirurgica |
Nella misurazione del dolore tra i due trattamenti l’intensità del dolore è più bassa nel gruppo trattamento. Il Danazolo presenta effetti indesiderati non trascurabili che ne consigliano l’uso in casi limitati. |
|
2007 Pub med |
Bahamondes et al |
Uso dei dispositivi intrauterini a base di levonorgestrel in donne con endometriosi, dolore pelvico cronico e dismenorrea |
1-42 donne |
Effetti sul dolore e sulle perdite ematiche dei dispositivi intrauterini e base di levonorgestrel |
Dispositivi intrauterini a base di GnRH analoghi sono efficaci, nella riduzione del dolore sulle perdite ematiche per un anno, cautela per un uso prolungato. |
|
2006 Pub Med
|
Attar et al |
Gli inibitori dell’aromatasi: la prossima generazione di farmaci per l’endometriosi? |
10-40 donne |
Effetti degli inibitori dell’aromatasi (AI) sulle donne affette da endometriosi,in particolare sul dolore pelvico cronico |
La terapia con gli inibitori dell’aromatasi ha una riuzione dei sintomi nelle donne affette da endometriosi. Rispetto agli analoghi è di più semplice gestione ha meno effetti collaterali, può essere utilizata per più tempo. |
|
2012 Pub Med
|
Champaneria et al |
Terapia psicologica per il dolore pelvico cronico: revisione degli studi clinici randomizzati |
nd |
Terapia psicologica e suo effetto sul dolore |
Punteggio medio alla VAS negli studi inclusi trattamento vs nessun trattamento rilevato in due dei tre studi inclusia tre e sei mesi: a 3 mesi valori medi: 2.89 vs 6.16; 4.34 vs 3.23 a 6 mesi valori medi: 2 vs 5.95; 3.76 vs 3.22
|
|
2008 Pub Med
|
Dalpiaz et al |
Dolore pelvico cronico nelle donne: ancora una sfida |
nd |
Trattamenti medici e chirurgici nel CPP |
Livello di raccomandazione 3/C nell’impiego di FANS, trattamenti ormonali ( GnRH agonisti), terapia fisica in associazione con analgesici, farmaci analgesici (amitriptilina)
|
|
2009 Pub Med |
Montenegro de Souza et al |
La sindrome del dolore miofasciale dell’addome deve essere considerata nella diagnosi differenziale del dolore pelvico cronico |
nd |
Valutare la presenza del dolore miofasciale nelle donne affette da CPP |
Nelle donne con CPP si rileva una compromissione dell’apparato scheletrico e muscolare e nel 15% di esse si associa la sindrome del dolore miofasciale. |
|
2010 Pub Med |
Mohedo- Diaz et al |
Considerazioni eziologiche, diagnostiche e erapeutiche della componente miofasciale nel dolore pelvico cronico |
4-50 |
Valutazione alterazioni: · posturali · muscolo scheletriche · presenza trigger point |
Riduzione del dolore tramite misurazione con VAS scale nei pazienti trattati con terapia fisica nelle zone di trigger con varie tecniche.
|
|
2010 Pub Med |
Parsons |
Il ruolo dell’epitelio permeabile e del potassio nella generazione dei sintomi vescicali nella cistite interstiziale / vescica iperattiva, sindrome uretrale, prostatite e dolore pelvico cronico ginecologico |
244 donne |
Viene utilizzato il Test di sensibilità del Potassio nelle donne affette da CPP e vengono valutate anche con la PUF |
80% delle donne sono risultate positive al Test del potassio. |
|
2009 Pub Med |
Abbot |
Indicazioni ginecologiche per l’uso della tossina botulinica nelle donne con dolore pelvico cronico |
200 donne |
Analisi sull’appropriatezza dell’uso delle iniezioni di botox nel punto di trigger point nelle donne con CPP |
l’uso del Botox riduce certamente la pressione sulla muscolatura pelvica, ma non sembra avere dei risultati significativi sul controllo e sulla riduzione del dolore come prima battuta nel CPP.
|
|
2007 Pub Med |
Montenegro et al |
Terapia psicologica nella gestione del dolore pelvico cronico nelle donne |
nd |
Blocco neuronale Iniezioni con tossina botulinica Elettrostimolazioni trans vaginali Stimolazioni tibiali percutanee intermittenti Terapia manuale transvaginale |
Blocco neuronale: effettivo nel 72% dei casi con 50% della riduzione del dolore; tossina botulinica: miglioramento nella VAS per dispaurenia ( 80vs28) e dismenorrea ( 67vs28) elettostimolazioni transvaginali: successo nel 50% dei casi trattati con riduzione alla VAS (83% vs 32%) stimolazioni tibiali percutanee: risposta positiva al dolore 42% con VAS <30 nel 21% dopo 12 settimane. Terapia manuale: riduzione significativa dei sintomi per 4-5 mes.i
|
|
2013 Pub Med |
Carinci et al |
Trattamenti complementari e alternativi nel dolore pelvico cronico |
20-30 donne per ogni studio incluso |
· agopuntura · fiterapia · massaggi · terapia mente/corpo |
Negli studi inclusi per ogni trattamento citato si è osservata una riduzione del dolore nel gruppo trattamento. Purtroppo gli studi considerati non sono Rct o non hanno mascheramento.
|
|
2011 Pub Med |
Lamvu |
Il ruolo dell’isterectomia nel trattamento del dolore pelvico cronico |
nd |
Viene valutata la ripresa dei sintomi, la qualità della vita, e la ricomparsa del dolore dopo l’isterectomia eseguita nel CPP
|
In una percentuale compresa tra il 21 ed il 40% delle donne il dolore ricompare dopo l’intervento, nel 5% dei casi il dolore aumenta. |
|
2011 Pub Med |
Hyun et al |
Gestione del dolore pelvico cronico |
nd |
Vengono analizzate patologie che possono determinare il CPP che sono: – endometriosi – cistite interstiziale – utero retroverso – sindrome della congestione pelvica – presenza delle aderenze – sindrome del dolore mio fasciale – sindrome del colon irritabile |
Nella cistite intesrstiziale i trattamenti che hanno effetti sul CPP sono quelli farmacologci e le instillazioni locali. Nell’endometriosi i trattamenti efficaci sul dolore sono quelli con Danazolo, GnRH analoghi, progestinici hanno effetto sul 80-90 % delle persone affette da CPP. Tra le terapie chirurgiche quelle che hanno più efficacia sono quelle laparoscopiche. l’ablazione del nervo presacrle è efficace nell’80% delle donne affette da dolore intermedio. L’isterectomia deve essere accompagnata a ovariectomia per diminuire la ricomparsa del dolore e la possibilità di recidive. Nella sindrome da congestione pelvica il dolore diminuisce in maniera significativa dopo terapia embolica (7.6 vs 2.9; p<0.0001) Nella terapia fisica le iniezioni nella zone di trigger point si sono dimostrate efficaci nel controllo del dolore.
|
|
2014 Pub Med |
Baranowski et al |
Il dolore pelvico cronico: un percorso per lo sviluppo delle cure sia negli uomini che nelle donne a cura della società britannica per il dolore |
nd |
Uso degli oppioidi; terapie interventistiche; terapia fisica |
Gli oppioidi possono apportare dei benefici nel dolore cronico, ma il loro utilizzo nel CPP è poco chiaro e va effettuato sotto controllo. Le iniezioni locali hanno efficacia nella diagnosi e nella gestione del dolore legato a problemi muscolari o lesioni de nervo. Il blocco neuronale ha dimostrato una efficacia limitatat nel tempo. La terapia fisica è indicata in caso di prevalenza di sintomi urologici. |
|
2011 Pub Med |
Bruckental |
Il dolore pelvico cronico: approccio alla diagnosi ed al trattamento |
nd |
– farmacologico – trattamenti complementari – chirurgici – non chirurgici |
In base ai livelli di raccomandazione nel CPP i trattamenti più indicati ( Liv. A) sono: contraccettivi orali, GnRH agonisti, FANS, progestinici.
|
|
2013 Pub Med |
Triolo et al |
Il dolore pelvico cronico nell’endometriosi: una panoramica |
nd |
· antidolorifici · terapie ormonali · chirurgiche |
Gli antidolorifici non sono efficai nel controllo del dolore da endometriosi Le terapie ormonali hanno dei risultati sovrapponibili nella gestione del dolore pelvico. che non consentono di preferire una tipologia ad un’altra. La terapia chirurgica laparoscopica e non, è gravata da una ricomparsa delle recidive nel 50-60% dei casi trattati dopo 5-7 aa. Le tecniche di ablazione dei nervi uterini e plesso ipogastrico non trovano beneficio nel CPP da endometriosi
|
|
2010 Pub Med |
Stratton et al |
Dolore pelvico cronico ed endometriosi: evidenze traslazionali della relazione e implicazioni |
nd |
· terapia ormonale · terapia chirurgica · anti TNFα · terapia analgesica |
Tra le terapie ormonali riducono il dolore: porgestinici, GnRH analoghi, contraccettivi orali, sistemi intrauterini al levonorgestrel , inibitori dell’aromatasi. Terapia chirurgica: presenta recidiva nel 50-70% dei casi dopo 5-7aa. L’ablazione del nervo uterino trova indicazioni nel CPP da dismenorrea. La terapia antalgica non trova indicazione nell’endometriosi Spostamento dell’attenzione dalle lesioni al dolore Implicazione del SNC nella genesi del dolore Vengono valutati gli effetti dei vari trattamenti in uso per il dolore da endometriosi. Si illustrano i nuovi trattamenti come l’utilizzo dei TNF che controllano e inibiscono l’angiogenesi e le reazioni immunologiche e infiammatorie. Si prende in considerazione il meccanismo della neoangiogenesi e dei GNF. |
|
2013 Cochrane
|
Lu et al |
Trattamenti anti TNFα per il dolore pelvico associato ad endometriosi (revisione) |
21 donne |
Farmaci anti TNFα: controllo del dolore, raffronto con altri farmaci, effetti indesiderati |
Non ci sono evidenze sugli effetti sul dolore Non ci sono evidenze su possibili effetti indesiderati Non ci sono evidenze sui benefici clinici nell’utilizzo dei farmaci anti TNF |
|
2012 Cochrane
|
Brown et al |
Progestinici e antiprogestinici per il dolore associato ad endometriosi |
nd |
Farmaci progestinic e antiprogestinici confrontati con altri farmaci ormonali utilizzati nel trattamento dell’endometriosi |
Non ci sono evidenze circa il beneficio nell’utilizzo dei progestinici e degli antiprogestinici sia orali che in depot rispetto alle altre terapie ormonali normalmente utilizzate |
|
2011 Cochrane
|
Zhu et al |
Agopuntura per il dolore nell’endometriosi |
nd |
Agopuntura nel dolore da endometriosi |
Vi sono limitate evidenze circa l’efficacia dell’agopuntura nell’endometriosi |
|
2014 Cochrane
|
Cheong et al |
Interventi non chirurgici per la gestione del dolore pelvico cronico |
750 donne |
Trattamenti medici Trattamenti psicologici Terapie complementari |
Terapia medica ormonale ha riscontrato beeficio relativamente al progestogen (progestinico) il goserelin (presenta una più lunga efficacia nei confronti del dolore. Terapia chirurgica e ablazione non si sono dimostrate efficaci. La psicoterapia e il conselling determinano rassicurazione. |
|
2005 Cochrane |
Stones et al |
Interventi per trattare il dolore pelvico cronico nelle donne |
nd |
Terapia medica, fisica, chirurgica, stili di vita, psicoterapia |
Terapia medica con progestogen è associata a riduzione del dolore durante il trattamento, mentre il goserelin ha una più lunga durata dei benefici. Il conselling è associato a una riduzione del dolore e un miglioramento dell’umore |
Risultati
I lavori scientifici inclusi nello studio (Tabelle 3 e 4) hanno evidenziato un approccio terapeutico non univoco di tipo multimodale e multidisciplinare, inoltre alcuni autori rivolgono la loro attenzione e la scelta della terapia o verso il controllo della sintomatologia e della qualità della vita, oppure verso la causa che determina il dolore pelvico cronico. Le principali modalità terapeutiche utilizzate sono:
Terapia farmacologica antalgica
La terapia farmacologica per il controllo del dolore da CPP prevede un approccio non dissimile da quello utilizzato per le altre forme di dolore cronico dove i FANS rappresentano il trattamento di prima scelta (21,22). Un altro farmaco usato spesso è il tramadolo che presenta una buona azione analgesica e un basso potenziale rischio di abuso (23,24). Anche gli antidepressivi sono usati in un contesto di trattamento multimodale per il dolore e altre patologie correlate, come l’ansia e la depressione (25). Un Rct di Corbellis (26) introduce palmitoiletanolamide che produce effetti sulle donne affette da endometriosi superiori a quelle dei FANS di nuova generazione (COX-2).Un altro Rct (27) sostiente l’utilizzo dei derivati dei cannabinoidi come terapia antalgica di supporto per l’endometriosi.
Terapia ormonale
Questa terapia trova impiego nella cura dell’endometriosi, la quale colpisce le donne affette da CPP tra il 71 e l’80% (28) e prevede la somministrazione di farmaci che inibiscono la produzione e la circolazione sanguigna di estrogeni ,che provocano la riduzione delle lesioni e conseguentemente la diminuzione del dolore di accompagnamento. I primi farmaci introdotti sono stati gli androgeni (Danazol), questi farmaci si sono dimostrati efficaci nel controllo del dolore, ma presentano degli effetti indesiderati quali: irsutismo, voce maschile, aumento ponderale, edemi, acne, crampi muscolari, spotting, depressione, insonnia ecc. (29). Altre tipologie di farmaci usati sono quelle che inducono ipoestrogenismo o che si pongono in antagonismo con gli estrogeni stessi. Le molecole introdotte sono i GnRH analoghi, i quali hanno un alto costo e un tempo limitato di utilizzo, a causa degli effetti indesiderati sulla mineralizzazione ossea (30-35).
I farmaci progestinici sono sostenuti da altri Rct poiché hanno effetti positivi sul dolore e un basso costo rispetto agli analoghi (36-40).
Un altro approccio per la gestione del dolore da endometriosi è dato dagli inibitori dell’aromatasi, l’uso di queste molecole ha ravvisato dei risultati significativi in pazienti refrattari ai trattamenti conservativi tradizionali (41-43).
Anche i FANS di nuova generazione come i COX-2 sono utili per la gestione del dolore dell’endometriosi (44). Infine un Rct (45) utilizza il Raloxifene definito anche SERMs (selective estrogen receptor modulators) il quale, pur essendo un estrogeno è in grado di avere un’azione selettiva (e perciò benefica) su alcuni tessuti senza avere effetti indesiderati, ciononostante questo farmaco non migliora l’outcome del dolore che ricompare precocemente. Una revisione (46) confronta l’utilizzo di farmaci a base di progestinici ed antiprogestinici nel controllo del dolore da endometriosi, senza ottenere delle evidenze tali da preferire l’impiego di uno anziché l’altro.
Terapia fisica
La terapia fisica nel CPP è rivolta verso aspetti clinici diversi che sono:
– il controllo della postura e dell’apparato locomotore
– la ricerca delle aree di debolezza della parete muscolare della zona pelvica
– la valutazione di zone di trigger point/aree di iperattività nella zona pelvica.
Per quanto riguarda il controllo della postura e della correlazione esistente tra l’apparato locomotore e il dolore pelvico cronico sono stati individuati studi clinici che prendono in considerazione il test di Mensendiech (47,48). Altri autori (49-51), anziché considerare l’approccio somatocognitivo mettono in risalto nei loro studi le differenze posturali.
L’associazione tra debolezza della parete muscolare pelvica e CPP è stata considerata da vari autori (52-55) che considerano anche l’importanza dell’esame fisico della paziente, attraverso la palpazione delle zone muscolari pelviche effettuata durante l’esame fisico utile per valutare i distretti muscolari dell’elevatore dell’ano, del piriforme e dell’otturatore interno (56).
L’esame fisico della paziente è utile anche per la rilevazione delle aree di innesco del dolore, dette anche zone trigger point, che possono dare origine alla sindrome del dolore miofasciale (57,58), i muscoli principalmente coinvolti sono anche in questo caso l’elevatore dell’ano, il pubococcigeo, puborettale, il piriforme e l’otturatore interno (50,59,60). L’orientamento terapeutico per questa sindrome riguarda l’utilizzo di farmaci anestetici (maggiormente bupivacaina o lidocaina) oppure botulino, che vengono iniettati direttamente nel trigger point (61-63).
Rimanendo nel contesto della terapia fisica, studi clinici hanno evidenziato un legame tra le alterazioni muscolari, la cistite interstiziale (IC) e il CPP (64-66), altri studi affrontano la correlazione tra IC ed endometriosi (67,68).
Terapia chirurgica
Ad essa appartengono il trattamento delle aderenze (69), l’isterectomia (70,71) e l’ablazione del nervo utero-sacrale laparoscopico (LUNA) (72,73). Uno studio osservazionale retrospettivo (74) cita l’utilizzo di tecniche laparoscopiche con posizionamento di rete nelle zone inguinali con debolezza muscolare.
Terapie complementari e alternative
Queste sono essenzialmente rappresentate dall’agopuntura e dalla fitoterapia. La letteratura riporta pochi studi sia relativi all’agopuntura in ragazze adolescenti (75,76) e un Rct (77), oltre che una revisione in cui viene incluso un unico studio relativo alla terapia nell’endometriosi (78), mentre per la fitoterapia è stato individuato in una rassegna (79) un solo Rct relativo all’impiego dei flavonoidi. Ulteriori tipi di approccio e management del dolore sono rappresentati dal counselling e dalla psicoterapia (80,81). Una revisione afferma che tra le terapie alternative la distensione delle zone pelviche dolorose ha una maggiore efficacia del counselling (82). Citazioni a parte per le terapie interventistiche (83) tra le quali si comprendono le tecniche di neuro modulazione, il blocco neuronale, la stimolazione percutanea del nervo tibiale, sacrale e pudendo, che possono essere efficaci. A supporto di queste tecniche è stato individuato un Rct dove venivano trattati con successo pazienti affetti da CPP tramite stimolazione del nervo tibiale (84).
Discussione
Lo scopo di questa revisione è stato quello di descrivere gli approcci terapeutici utilizzati nella gestione del CPP. Il controllo del dolore diviene necessario, in quanto in alcune donne la sintomatologia-malattia dolorosa può assumere caratteristiche invalidanti, con un impatto negativo sulla qualità della vita, in particolare interferendo con l’attività sessuale, lavorativa, la minzione (57,79,82,83). Inoltre, il dolore può avere implicazioni negative sulla salute psicologica, associata a depressione, ansia, insonnia, difficoltà nell’esercizio lavorativo, e può addirittura determinare isolamento sociale (85).
Una delle peculiarità del dolore pelvico cronico è quella di assumere caratteristiche enigmatiche, o comunque poco chiare, sul meccanismo fisiopatologico che lo determina, in quanto molti dei suoi segni e sintomi possono manifestarsi anatomicamente al di fuori della pelvi (85). La sua eziologia è spesso non chiara e l’origine sembra essere multifattoriale, in virtù del coinvolgimento degli organi intra ed extra pelvici (86).
L’analisi della letteratura, inclusa nel nostro studio, ha evidenziato che il CPP risulta essere ancora una patologia di difficile inquadramento diagnostico, tanto è vero che oltre il 50% delle donne non riceve una diagnosi precisa (56,83).
Queste difficoltà che caratterizzano il dolore pelvico, relativamente alla diagnosi ed eziologia, si ritrovano analogamente nelle altre forme di dolore cronico (87), dove, come nel dolore pelvico, la caratteristica preminente è rappresentata dal concetto di inabilità e disabilità, che in generale si accompagna ad alterazioni dell’umore, del modo di essere, con ripercussioni sullo situazione economica e familiare (88). La gestione della qualità della vita, più che della patologia in sé e per sé, diviene un problema fondamentale per questi pazienti, suggerendo come paradigma un modello di approccio fondato sulla persona più che sulla patologia. Un modello biopsicosociale, quindi multimodale e multidisciplinare, si è dimostrato più efficace nella gestione del dolore cronico. Una delle problematiche maggiori, infatti, è rappresentata dal fatto che nel dolore cronico nessun trattamento sembra avere forti evidenze di base circa la sua efficacia rispetto ad altri (89).
Questa revisione ha fatto emergere innumerevoli pubblicazioni di fonti primarie, quali Rct (n.18), studi osservazionali (n.10), e secondarie, quali revisioni narrative (n. 23), revisioni sistematiche (2) e una metanalisi. Tali studi, in particolare quelli secondari, concordano sulle varie opzioni terapeutiche integrabili tra loro, utili al controllo e alla gestione del dolore pelvico. Gli approcci consigliati possono essere monodisciplinari, seguiti generalmente dallo specialista ginecologo, o in molti casi si ritiene vantaggioso e raccomandato un approccio multi-professionale e multidimensionale (90-94), in accordo con quanto già definito nell’ambito del dolore cronico. In questo contesto, il team potrà essere composto da vari professionisti, quali il ginecologo, l’anestesista specializzato in terapia antalgica (algologo), il fisioterapista, l’infermiere, lo psicologo (95).
Ad oggi, molte società scientifiche hanno dato indicazioni in merito alla classificazione, valutazione e gestione del CPP: l’American College of Obstetricians and Gynecologist (15); la Society of Obstetricians and Gynecologist of Canada (19); l’European Association of Urology (16), al fine di uniformare e di indirizzare le pazienti verso gli specialisti più appropriati. Data però la complessità del fenomeno, dal punto di vista diagnostico e terapeutico, persiste ancora una notevole variabilità di trattamenti. Pertanto, con il contributo della British Pain Society (2014), si è definito un percorso clinico in grado di indirizzare gli specialisti a trattamenti appropriati (96).
Le opzioni terapeutiche possono essere dirette verso una singola patologia, come l’endometriosi, in cui ci si avvale prevalentemente della terapia ormonale. L’utilizzo degli ormoni, diretto soprattutto al controllo del dolore e della proliferazione delle zone ectopiche, presenta delle problematiche non trascurabili che prendono in considerazione sia gli effetti indesiderati, in particolare l’alterazione della mineralizzazione ossea, sia la qualità delle perdite uterine, che l’economicità del farmaco e la capacità di gestione dello stesso da parte delle pazienti (46). I farmaci di nuova generazione come i TNFα (97-98), con i quali l’interesse si è spostato dal controllo della proliferazione ectopica al sintomo dolore, sembrano non essere efficaci (99).
La terapia chirurgica (isterectomia) e l’ablazione non risultano essere efficaci per il trattamento del dolore da endometriosi, in quanto la sintomatologia algica si può ripresentare indipendentemente dalla tecnica utilizzata (98).
In generale, la terapia fisica si inserisce all’interno di un approccio multidisciplinare integrato, dove possono essere utili approcci non farmacologici nel sollievo dal dolore definiti come medicina alternativa e complementare (CAM). CAM è un termine usato negli Stati Uniti, a cui si fa riferimento per descrivere un’ampia scelta di pratiche sanitarie, sistemi e prodotti che non fanno parte della cultura di un Paese, o che non sono integrati nel sistema dominante dell’assistenza sanitaria (100-101). In realtà, parlare di confini tra le CAM e la cosiddetta medicina convenzionale non è corretto e specifici trattamenti non convenzionali sono stati ampiamente accettati (101).
Le terapie complementari trovano un impiego sempre più crescente in varie forme di dolore cronico relativo a dolori muscolo-scheletrici (collo, schiena) (102) Anche in Italia questo tipo di terapia è in netto aumento, i trattamenti più utilizzati sono agopuntura, omeopatia e fitoterapia (103). Uno dei limiti delle CAM, nel nostro studio è quello di non essere supportate da dati generalizzabili, in quanto si tratta di studi eseguiti su piccoli campioni, e pertanto non supportati da forti evidenze scientifiche (79).
Tra i trattamenti farmacologici i FANS non sono considerati più farmaci di prima scelta, poiché non trovano un razionale nell’impiego dell’endometriosi. Anche gli oppiacei, a differenza di altre forme di dolore cronico, non trovano riscontro nel CPP, anche in virtù dell’iperalgesia indotta e dalle possibili alterazioni del sistema endocrino con relativa riduzione dei livelli degli ormoni sessuali (96). I farmaci che possono trovare impiego sono gli antidepressivi e gli anticonvulsivanti, che garantiscono un certo sollievo dal dolore (93).
Nei casi in cui il CPP sia correlato a cistite interstiziale, i trattamenti prevedono in primis l’uso di una dietoterapia, seguito dai trattamenti farmacologici, e le instillazioni vescicali (104).
Implicazioni per la pratica infermieristica
Le implicazioni per la pratica infermieristica sono chiaramente dipendenti dal fatto che l’approccio consigliato dalle linee guida è di tipo multidisciplinare, in virtù della complessa condizione che genera il CPP, offrendo simultaneamente assistenza e gestione nella componente somatica, comportamentale e psicosociale del dolore. Il target del team rimane essenzialmente quello di identificare le cause che determinano il CPP,controllare il dolore, migliorare la qualità di vita, ed è proprio sul suo miglioramento che il team assistenziale deve puntare (105), prendendo come riferimento un approccio di tipo olistico che tenda dove è possibile alla riduzione del dolore, ma che consideri il controllo delle disfunzioni fisiche e psicologiche (106) . L’infermiere, dato il modello concettuale paradigmatico di tipo bio-psico-sociale su cui fonda le sue teorie, è colui che è più indicato a supportare e guidare questo tipo di iniziative (107). Si veda il modello di Gordon (108), dove effettivamente vengono presi in considerazione tutti i vari aspetti utili nel miglioramento della qualità della vita delle persone.
In particolare, le attività infermieristiche saranno indirizzate su più fronti quali: la valutazione dei sintomi, l’adesione al regime terapeutico e il monitoraggio degli effetti collaterali, la gestione della dieta.
La valutazione dei sintomi, dove non va considerata solo la componente algica, si realizza tramite appositi strumenti. In particolare le disfunzioni del tratto urinario che caratterizzano la cistite interstiziale si valutano attraverso varie scale: la O’ Leary-Sant IC Symptom and Problem Index (109) misura la severità dei sintomi della cistite intestiziale. È composta da due scale: la Symptom Index che misura l’urgenza e il dolore, e la Problem Index, che misura l’esperienza del paziente per ogni sintomo. Un punteggio minimo di sei per ogni scala è indicativo di cistite interstiziale (110).
Sebbene questa scala non costituisca uno strumento di screening, può essere usata per chiarire la diagnosi e nella gestione della IC (110-111).
Un’altra scala utilizzata è la Pelvic Pain and Urgency/Frequency Patient Symptom Scale, è una scala di screening che misura il dolore e l’urgenza nella minzione. Anch’essa è composta da due scale: il punteggio dei sintomi misura l’accordo dei sintomi col paziente, e la misura della preoccupazione legata al fastidio (112).
La Pelvic Pain and Urgency/Frequency Patient Symptom Scale può essere usata per identificare l’insieme dei sintomi ed i pazienti che hanno probabilità di avere la IC/BPS. E’ composta da una sola pagina e la sua compilazione richiede meno di cinque minuti da parte dei pazienti ed è utile sia nella diagnosi che nel follow up del trattamento (112).
Un altro strumento usato è il diario minzionale, che in genere deve essere redatto dal paziente da 1 a 4 settimane, almeno inizialmente. Con il diario il paziente terrà traccia di quando e quanto riescono a mingere, oltre che il tasso e il livello del dolore associato alla minzione, così come ogni fattore che acuisce o pallia il dolore. Più a lungo viene mantenuto il diario e maggiore chiarezza sui sintomi può essere fatta, inoltre può dare indicazioni anche per la validità dei trattamenti che vengono instaurati (104).
La valutazione sul paziente deve comprendere anche altri aspetti, come il livello d’ansia e depressione, le alterazioni della sessualità; in tal caso l’infermiere dovrà indirizzare il paziente verso le figure professionali del team che meglio possono supportarlo, come lo psicologo o lo psichiatra e il sessuologo.
Nel regime educativo potranno essere affrontate le problematiche relative agli effetti collaterali dei farmaci, come i potenziali effetti gastrolesivi dei FANS, o istruire i pazienti circa le possibili alterazioni della mineralizzazione ossea.
La prosecuzione dell’utilizzo di strumenti come il diario minzionale rimane di importanza strategica, poiché valuta l’efficacia del trattamento utilizzato, così come il rispetto dei regimi dietetici (104).
Nella gestione del dolore vanno considerate la capacità di istruire il paziente nel saper agire sul volume e sulla concentrazione delle urine (113). Se l’aumento del volume delle urine può determinare un aumento della soglia del dolore, una sua diminuzione può mitigare la risposta al dolore, per contro, anche l’aumento della concentrazione delle urine può causare una increzione dei livelli di potassio. Questo determina sulla vescica uno stimolo irritativo che causa dolore, quindi se si aumenta l’idratazione si abbassa la soglia del dolore.
Il paziente dovrà autonomamente essere in grado, attraverso la sperimentazione, di personalizzare l’intake dei fluidi con l’intento di migliorare la risposta al dolore.
Altro aspetto è la dieta: questa riveste un duplice aspetto sia diagnostico che terapeutico. Il dolore pelvico, l’urgenza minzionale e la sua frequenza diminuiscono con l’eliminazione degli alimenti irritanti dalla dieta. Alcuni dei cibi cosiddetti irritanti includono: formaggi stagionati, yogurt, cioccolato, cipolle, prodotti alla soia, pomodori, vari tipi di frutta (all’infuori di melone, mirtilli e pere), pane di segale, nocciole (eccetto gli anacardi e le mandorle), bevande alcoliche, caffè, bibite, succhi di frutta, maionese, ketchup, mostarda, spezie, la maggior parte dei conservanti, dolcificanti artificiali e tabacco (114-115). Ai pazienti viene fornito un volantino con gli alimenti divisi in gruppi. Nella lista vengono indicati i cibi irritanti e quelli non irritanti. La dieta vene iniziata solo con i cibi non irritanti da cui ci si aspetta un miglioramento dei sintomi dopo circa un mese. Successivamente vengono introdotti uno alla volta i cibi preferiti dal paziente, se il dolore ritorna l’alimento introdotto deve essere eliminato. Naturalmente l’adesione alla dieta è un processo difficile e lungo, a cui si deve associare il diario minzionale, per verificare la modifica della qualità del dolore associato al cambiamento dietetico, dolore inteso come esacerbazione o riduzione dei sintomi.
Un altro aspetto della terapia educazionale è rappresentato dall’introduzione delle fibre nella dieta, oltre alla giusta idratazione. Le persone con CPP devono evitare i cibi che causano irritabilità al pavimento della vescica e considerare che la debolezza delle pareti muscolari, la mancanza di esercizio fisico possono determinare fenomeni di stitichezza che acuiscono il dolore.
Conclusioni
L’obiettivo di partenza di questa revisione era quello di descrivere i trattamenti idonei e più indicati nella gestione del dolore pelvico cronico, la ricerca ha ancora una volta evidenziato la valenza nella gestione multidisciplinare e multidimensionale del CPP. Infatti le ultime evidenze propendono oltre che a sottolineare i vari criteri di classificazione della patologia, a includerla in un percorso diagnostico terapeutico.
All’interno dell’équipe, tra le figure non mediche l’infermiere assume un ruolo definito e a volte determinante sia nelle fasi di inquadramento diagnostico che nel follow up della patologia, in particolare nel controllo dei disturbi urinari. Purtroppo in Italia, alla luce della legge 38/2010, non esiste a tutt’oggi un ruolo definito e strutturato nella gestione delle donne con CPP, come lo è in altri Paesi, dove addirittura si ipotizza la possibilità di affidare all’infermiere la gestione dell’équipe multiprofessionale proprio per la visione olistica che caratterizza la professione.
Bibliografia
1. Williams RE, Hartmann KE, Steege JF. Documenting the current definitions of chronic pelvic pain: Implications for research. Obstet Gynecol 2004;103:686–91.
2. Stones RW, Price C. Health services for women with chronic pelvic pain. J R Soc Med 2002; 95(11): 531–535.
3. Campbell F, Collett BJ. Chronic pelvic pain. Br J Anaesth 1994;73:571–573.
4. Zondervan K, Barlow DH. Epidemiology of chronic pelvic pain. Best Pract Res Clin Obstet Gynaecol 2000;14:403–414.
5. Howard FM. Chronic pelvic pain. Obstet Gynecol. 2003;101: 594–611.
6. Myers DL, Aguilar VC. Gynecologic manifestations of interstitial cystitis. Clin Obstet Gynecol. 2002;45(1):233–241).
7. Pagano de Oliveira Goncalves da Silva G, do Nascimento AL, Michelazzo D, et al. High prevalence of chronic pelvic pain in women in Ribeirao Preto, Brazil and direct association with abdominal surgery. Clinics 2011;66(8):1307-1312.
8. Latthe P, LattheM, Say L, Gulmezoglu M, Khan KS. WHO systematic review of prevalence of chronic pelvic pain: a neglected reproductive health morbidity . BMC public health, 2004;28:369-75.
9. Bartoletti R, Cai T, MondainiN, et al. Prevalence, incidence estimation, risk factors and characterization of chronic prostatitis/chronic pelvic pain syndrome in urological hospital outpatients in Italy: results of a multicenter case-control observational study. J Urol 2007;178 (6), 2411–2415.
10. Ahangari A. Prevalence of chronic pelvic pain among women: an update rewiev. Pain Physician 2014;17:E141-E147
11. Evans S. Chronic pelvic pain in Australia and New Zealand. Aust N Z J Obstet Gynaecol 2012; 52:499- 501.
12. Romao APMS, Goyareb R, Romano G, Poli-Neto OB, dos Reis FJC, Rosa e Silva JC, Nogueira AA. High levels of anxiety and depression have a negative effect on quality of life of women with chronic pelvic pain. Int J Clin Pract 2009;63:707-711.
13. Mathias SD, Kuppermann M, Liberman RF, Lipschutz RC, Steege JF. Chronic pelvic pain: prevalence, health-related quality of life and economic correlates. Obstet Gynecol 1996; 87(3), 321-327.
14. Moore J, Kennedy S. Causes of chronic pelvic pain. Baillieres Best Pract Res Clin Obstet Gynaecol 2000;14(3):389-402.
15. ACOG Committee on Practice Bulletins-Gynecology. ACOG Practice Bulletin No.51. Chronic pelvic pain. Obstet Gynecol2004; 103(3):589-605.
16. Fall M, Baranowski AP, Fowler CJ, Elneil S, Hughes J, Messelink EJ, de C Williams AC. EAU guidelines on chronic pelvic. European Urology 2010; 57(1):35-48.
17. Fall M, Baranowski AP, Fowler C J, Lepinard V, Malone –Lee JC, Messelink EJ, et al. European Association of Urology. EAU guidelines on chronic pelvic. Eur Urol 2004; 46(6):681-689.
18. Dick ML. Chronic pelvic pain in women: assessment and management. Australian Family Physician 2004; 12(33):971-976.
19. Jarrell JF, Vilos GA,Albaire C, and Chronic Pelvic Pain Working Group, SOGC. Consensus guidelines for the management of chronic pelvic pain. J Obstet Gynaecol Can 2005; 27(8): 781-826.
20. Ortiz DD. Chroni pelvic pain in women. Am Fam Physician 2008;77(11): 1535-1542.
21. Bordman R, Jackson B. Below the belt. Approach to pelvic pain. Can Fam Physician 2006;52:1556-1562.
22. Green IC, Cohen SL,Finkenzeller D, Christo PJ. Interventional therapies for controlling pelvic pain: what is the evidence? Curr Pain Headache Rep 2010; 14:22-32.
23. Adams EH, Breiner S, Cicero TJ, et al. A comparison of the abuse liability of tramadol, NSAIDs, and hydrocodone in patients with chronic pain. J Pain Symptom Manage 2006, 31:455–476.
24. Chou R, Clark E, Helfand M. Comparative efficacy and safety of long-acting oral opioids for chronic non-cancer pain: a systematic review. J Pain Symptom Manage 2003, 26:1026–1048.
25. Bajwa ZH, Simopoulos TT, Pal J, et al. Lowand therapeutic doses of antidepressants are associated with similar response in the context ofmultimodal treatment of pain. Pain Physician 2009, 12:893–900.
26. Corbellis L, Castaldi MA, Giordano V, Trabucco E, De Francisis P, Torella M, Colacurci N. Effectiveness of the association micronized N-Palmitoylethanolamine(PEA)–transpolydatin in the treatment of chronic pelvic pain related toendometriosis after laparoscopic assessment: a pilot study. Eur J Obstet Gynecol Reprod Bio 2011; 158:82-86
27. Giugliano E, Cagnazzo E, Soave I, Lo Monte G, Wenger JM, Marci R. The adjuvant use of N-palmitoylethanolamine and transpolydatin in the treatmeny of endometriotic pain. Eur J Obstet Gynecol Reprod Bio 2013; 168:209-213.
28. Ozawa Y, Murakami T, Terada Y, Yaegashi N, Okamura K, Kuriyama S, Tsuji I. Management of the pain associated with endometriosis : an update of the painful problems. J Exp Med 2006;210(3):175-188
29. Farquhar C, Prentice A, Singla AA, Selak V. Danazol for pelvic pain associated with endometriosis(Review). The Cochrane Library 2007 Issue 4.
30. Ailawandi RK, Jobanputra S, Kataria M,Gurates B, Bulun SE. Treatment of endometrios and chronic pelvic pain with letrozole and norethindrone acetate: a pilot study. Fertil Steril 2004;2: 290-296.
31. Guzick DS, Li-S Huang, Broadman BA, Nealon M, Hornstein MD. Randomized trial of leuprolide versus continuos oral contraceptives in the treatment of endometriosis-associated pelvic pain. Fertil Steril 2011;95(5):1568-1573.
32. Petta CA, Ferriani RA, Abrao MS, Hassan D, Rosa e Silva YC, Podgaec S, Bahamodes L. Randomized clinical trial of a levonorgestel-releasing intrauterine system and a depot GnRH analogue for the treatment of chronic pelvic pain in women with endometriosis. Hum Reprod 2005;20(7):1993-1998.
33. Bahamondes L, Petta CA, Fernandes A, Monteiro I. Use of the levonogestrel- releasing intrauterine system in women with endometriosis, chronic pelvic pain and dysmenorrhea. Contraception 2007;75: S134-S139.
34. Fedele L, Bianchi S, Zanconato G, Portuese A, Raffaelli R. Use of levonogestrel-releasing intrauterine device in the treatment of rectovaginal endometriosis. Fertil Steril 2001;75: 485-8.
35. Bayoglu YT, Dilbaz B, Altinbas SK., Dilbaz S. Postoperative medical treatment of chronic pelvic pain related to severe endometriosis: levononogestrel-releasing intrauterine system versus gonadotropin-releasing hormon analogue. Fertil Steril 2011; 95(2): 492-496.
36. Razzi S, Luisi S, Ferretti C, Calonaci F, Gabbanini M, Mazzini M, Petraglia F. Use of progestogen only preparation containing desogestrel in the treatment of recurrent pevic pain after conservative surgery for endometriosis. Eur J Obstet Gynecol Reprod Biol 2007; 135: 188-190.
37. Harada T, Momoeda M, Taketani Y, Aso T, Fukunaga M, Hagino H, Terakawa N. Dienogest is as effective as intranasal buserelin acetate for the relief of pain syntoms associated with endometriosis- a randomized, double-blind, multicenter, controlled trial. Fertil Steril 2009;91(3):675-681.
38. Strowitzki T, Faustmann T, Gerlinger C, Seitz C. Dienogest in the treatment of endometriosis- associated pelvic pain: a 12-week, randomized, double-blind, placebo-controlled study. Eur J Obstet Gynecol Reprod Biol 2010; 151.
39. Kitawaki J, Kusuki I, Yamanaka K, Suganuma I. Maitenance therapy with dienogest following gonadotropin-releasing hormone agonist treatment for endometriosis-associated pelvic pain. Eur J Obstet Gynecol Reprod Biol 2011; 157: 212-216.
40. Cheong YC, Smotra G, Williams ACDC. Non surgical interventions for the management of chronic pelvic pain (Review). The Cochrane Library 2014, Issue 3.
41. Attar E, Bulun SE. Aromatase inhibitors: the next generation of therapeutics for endometriosis? Fertil Steril 2006; 85(5): 1307-1318.
42. Abushahin F, Goldman KN, Barbieri E, Milad M, Rademaker A, Bulun SE. Aromatase inhibition for refractory endometriosis-related chronic pelvic pain. Fertil Steril 2011; 96(4): 936-942.
43. Verma A, Konje JC. Successful treatment of refactory endometrosis-related chronic pelvic pain with aromatase inhibitors in premenopausal patients. Eur J Obstet Gynecol Reprod Biol 2009; 143: 112-115.
44. Cobellis L, Razzi S, De Simone S, Sartini A, Fava A, Danero S, Gioffrè W, Mazzini M, Petraglia F. The treatment with COX-2 specific inhibitor is effective in the management of pain related to endometriosis. European Journal of Obstetrics & Ginecology and Reproductive Biology 2004; 116: 100-102.
45. Stratton P, Sinaii N, Segars J, Koziol D, Wesley R, Zimmer C, Winkel C, Nieman KL. Return of Chronic Pelvic Pain From Endometriosis After Raloxifene Treatment:A Randomized Controlled Trial. Obstet Gynecol. 2008 ; 111(1): 88–96.
46. Brown J, Kives S,Akhtar M. Progestagens and anti-progestagens for pain associated with endometriosis (Review).The Cochrane Library. 2012, Issue 3.
47. Haugstad GK, Haugstad TS, Kirste UM, Leganger S,Wojniusz S, Klemmetsen I, Malt UF. Posture, movement patterns, and body awareness in women with chronic pelvic pain. J Psychosom Res. 2006; 61: 637-644.
48. Haugstad GK, Haugstad TS, Kirste UM, Leganger S,Wojniusz S, Klemmetsen I, Malt UF. Continuing improvement of chronic pelvic pain in women after short-term Mensendieck somatocognitive therapy: a results of a 1-year follow-up study. Am J Obstet Gynecol 2008;615:e1-e8.
49. Montenegro MLLS, Mateus-Vasconcelos ECL, Rosa e Silva JC, Candido dos Reis F, Nogueira AA, Poli-Neto OB.Postural cenge in women with chronic pelvic pain: a case control study. BMC Musculoskeletal Disord 2009; 10(82):1-4
50. Neville CE, Fitzgerald CM, Mallinson T, Badillo S, Hynes C, Tu F. A preliminary report of musculoskeletal dysfunction in female chronic pelvic pain: a blinded study of examination findings. J Bodyw Mov Ther 2011; 16:50-56
51. Kaercher WC, Gerno VK, Souza CA, Alfonsin M, Berton G, Cunha Filho J. Baropodometry on women suffering from chronic pelvic pain-a cross-sectional study BMC Women’s Health 2011; 11(51): 1-5.
52. Tu FF, Holt J, Gonzales J, Fitzgerald CM. Physical therapy evaluation of patients with chronic pelvic pain: a controlled study. Am J Obstet Gynecol 2008;198:272:e1-e7.
53. Montenegro M LLS, Mateus-Vasconcelos E CL, Rosa e Silva JC, Candido dos Reis F, Nogueira A, Poli-Neto OB. Importance of pelvic muscle tenderness evaluation in women with chronic pelvic pain. Pain Medicine 2010; 11; 224-228.
54. Montenegro M LLS, Mateus-Vasconcelos E CL, Rosa e Silva JC, Candido dos Reis F, Nogueira A, Poli-Neto OB. Thiele massage as a therapeutic option for women with chronic pelvic pain caused by tenderness of pelvic floor muscles. J Eval Clin Pract 2010;16:981-982.
55. Heyman J, Öhrvik J, Leppert J. Distention of painful structures in the treatment for chronic pelvic pain in women. Acta Obstet Gynecol Scand 2006;85:599-603.
56. Montenegro M LLS, Gomide LB, Mateus-Vasconcelos E CL, Rosa e Silva JC, Candido dos Reis F, Nogueira A, Poli-Neto OB. Abdominal myofascial pain syndrome must be considered in the differential diagnosis of chronic pelvic pain. Eur J Obstet Gynecol Reprod Biol. 2009;147:21-24.
57. Mohedo-Diaz E, Lopez-Baron FJ, Pineda-Galan C. Etiological, diagnostic and therapeutic consideration of the myofascial component in chronic pelvic pain. Actas Urol Esp. 2011;35(10):610-614.
58. Gyang A, Hartman M, Lamvu G. Musculoskeletal causes of chronic pelvic pain. Obstet Gynecol 2013; 121 (3):645-650.
59. Slocumb JC. Neurologic factors in chronic pelvic pain: trigger points and the abdominal pelvic pain syndrome. Am J Obstet Gynecol 1984;149:536-43.
60. Carter JE. Surgical treatment for chronic pelvic pain. JSLS 1998:2:129–39.
61. Langford C, Nagy US, Ghoniem GM. Levator ani trigger point injections: an underutilized treatment for chronic pelvic pain. Neurourol & Urodyn 2007; 26:59-62.
62. Abbott J. Gynecological indications for the use of botulinum toxin in women with chornic pelvic pain Toxicon 2009; 54:647-653.
63. Nesbitt-Hawes EM, Won H, Jarvis SK, Lyons SD, Vancaillie TG, Abbott JA. Improvement in pelvic pain with botulinum toxine type A- single vs repeat injections. Toxicon 2013;63:83-87.
64. Paulson JD, Paulson JN. Anterior vaginal wall tenderness (AVWT) as a physical symptom in chronic pelvic pain. JSLS 2011;15: 6-9.
65. Parsons LC. The role of leaky epithelium and potassium in the generation of bladder symptoms in interstitial cystitis/overactive bladder, urethral syndrome, prostatitis and gynaecological chronic pelvic pain. BJU International 2010;107:370-375.
66. Fitzgerald MP, Payne CK, Lukacz ES, Yang CC, Peters KM, et al. Randomized multicenter clinical trial of myofascialphysical therapy in women with interstitial cystitis/painful bladder syndrome and pelvic floor tenderness. J Urol 2012; 187.2113-2118.
67. Chung MK. Intestitial cystitis in persistent posthysterectomy chronic pelvic pain. JSLS 2004;8:329-333.
68. Cheng C, Rosamilia A, Healey M. Diagnosis of interstitial cystitis/bladder pain syndrome in women with chronic pelvic pain: a prospective observational study. Int Urogynecol J 2012; 23:1361-1366.
69. Keltz MD, Gera PS, Olive DL. Prospective randomized trial of right-sided paracolic adhesiolysis for chronic pelvic pain. JSLS 2006;10:443-446.
70. Lamvu G. Role of hysterectomy in the treatment of chronic pelvic pain. Obstet Gynecol2011; 117 (5):1175-1178.
71. Shin JH, Howard FM. Management of Chronic Pelvic Pain. Curr Pain Headache Rep 2011; 15:377–385.
72. Daniel J, Gray R, Hills RK, Latthe P, Buckley L, Gupta J, Selman T, Adey E, Xiong T, Champaneria R, Lilford R, Khan S K.. Laparoscopic uterosacral nerve ablation for alleviating chronic pelvic pain. JAMA 2009; 302(9):955-961.
73. Xiong T, Daniels J, Middleton L, Champaneria R, Khan KS, Gray R, Johnson N, Lichten EM, Sutton C, Jones KD, Chen F-P, Vercellini P, Aimi G, Lui W-M on behalf of the International LUNA IPD Meta-analysis Collaborative Group. Meta analysis using individual patient data from randomised trials to assess the effectiveness of laparosopic uterosacral nerve ablation in the treatment of chronic pelvic pain: a proposed protocol. BOJG 2007;114:e1-e7.
74. Yong PJ, Williams C, Allaire C. Laparoscopic inguinal exploration and mesh placement for chronic pelvic pain. JSLS 2013;17:74-81.
75. Conboy L, Quilty MT, Kerr C, Shaw J, Wayne P. A qualitative analysis of adolescents’ experiences of active and sham Japanese-style acupuncture protocols administered in a clinical trial. J Altern Complement Med 2008 Jul;14(6):699-705.
76. Schnyer RN, Iuliano D, Kay J, Shields M, Wayne P. Development of protocols for randomized sham-controlled trials of complex treatment interventions: Japanese acupuncture for endometriosis-related pelvic pain. J Altern Complement Med 2008 Jun;14(5):515-22.
77. Ozel S, Arsland H, Kocak Z., Tufan KZ, Uzunkulaoglu T, Akarsu D, Seven A. Acupunture in the treatment of chronic pain secondary to pelvic inflammatory disease. Acupunt Med 2011 ;29(4):317-318.
78. Zhu X, Hamilton KD, McNicol MD. Acupunture for pain in endometriosis ( Review) The Cochrane Library 2011, Issue 9.
79. Carinci AJ, Pathak R, Young M, Christo PJ. Complementary and alternative treatments for chronic pelvic pain. Curr Pain Headache Rep 2013;7;316:1-5.
80. Stones W, Cheong YC, Howard FM, Singh S. Interventions for treating chronic pelvic pain in women. Cochrane Library 2005, Issue 2.
81. Champaneria R, Daniels JP, Raza A, Pattison HM, Khan K.S. Psycological therapies for chronic pelvic pain: systematic review of randomized controlled trials. Acta Obstet Gynecol Scand 2012;91:281-286
82. Cheong YC, Smotra G, Williams ACDC. Non- surgical interventions for the management of chronic pelvic pain. Cochrane Library 2014, Issue 3.
83. Baranovski AP. Chronic pelvic pain. Best Pract Res Clin Gastroenterol 2009; 23: 593–610
84. Kim SW, Paik JS, Ku JH. Percutaneous posterior tibila nerve stimulation in patients with chronic pelvic pain: a preliminary study. Urol Int 2007;78:58-62.
85. Nickel JC, Tripp DA, Pontari M, Moldwin R, Mayer R, Carr LK, Doggweiler R, Yang CC, Mishra N, Nordling J. Interstitial cystitis/painful bladder syndrome and associated medical conditions with an emphasis on irritable bowel syndrome, fibromyalgia and chronic fatigue syndrome. J Urol 2010;184(4):1358-63.
86. Peters AAW,Van den Tilaart SAHM. The difficult patient in gastroenterology: Chronic pelvic pain, adhesions, and subocclusive episodes. Best Practice and research clinical gastroenterology 2007;21(3):445-463.
87. Merskey H, Bogduk N. Classification of chronic pelvic pain: description of chronic pain syndromes and definition of pain terms. Seattle: IASP Press;1994
88. Scottish Intercollegiate Guidelines Network (SIGN). Management of chronic pain. Edinburgh: SIGN; 2013.
89. IASP Interdisciplinary chronic pain management: international perspective. IASP newsletter 2012;20, issue 7.
90. Butrick CW. Chronic pelvic pain how many surgeries are enough? Clin Obstet Gynecol 2007;50(2):412-424.
91. Daniels JP, Middleton L, Xiong T, Champaneria R, Johson NP, Lichten EM. International LUNA IPD Meta- analysis Collaborative Group. Individual patient data meta-analysis of randomized evidence to assess the effectiveness of a laparoscopic uterosacral nerve ablation in chronic pelvic pain. Human Reprod Update 2010;16(6):568-576.
92. Gunter J. Chronic pelvic pain: An integrated approach to diagnosis and treatment. Obstet Gynecol Survey 2003;58(9):615-623.
93. Bruckental P. Chronic pelvic pain: approaches to diagnosis and treatment. Pain Manag Nursing. 2011; 12 (1):s4-s10
94. Dalpiaz O, Kerschbaumer A, Mitterberger M, Pinggera G, Bartsch G, Strasser H. Chronic pelvic pain in women: still a challenge. BJU International 2008; 102: 1061-1065.
95. Weisender CCT Pelvic pain clinic: a multidisciplinary approach, In: Li T, Ledger W (eds). Chronic pelvic pain, Taylor and Francis. London: 197-210.
96. Baranowski AP, Lee J, Price C, Hughes J. Pelvic pain: a pathway for care developed for both men and women by the British Pain Society. Br J Anaesth 2014;112(3):452-9.
97.Triolo O, Laganà AS, Sturlese E. Chronic Pelvic Pain in Endometriosis: An Overview. Clin Med Res 2013;5(3):153-163
98. Stratton P, Berkley K.J. Chronic pelvic pain and endometriosis: translational evidence of the relationship and implications Human Reprod Update 2011;17:327–346.
99. Lu D, Song H, Shi G. Anti-TNF-α treatment for pelvic pain associated with endometriosis. Cochrane Library 2013 Issue 3.
100. National Center for Complementary and Alternative Medicine 2015. https://nccih.nih.gov/health/whatiscam. Accessed Jan. 2015.
101. World Health Organization: Traditional Medicine 2015. http://goo.gl/PSud21. Accessed Jan. 2015
102. Barnes PM, Bloom B, Nahin RL. Complementary and alternative medicine use among adults and children: United States, 2007. Natl Health Sta Rep 2008;12:1-23.
103. Menniti-Ippolito F, Bologna E, Gargiulo L, Forcella E, Sabbadini LL, Raschetti R. Characteristics of unconventional medicine users and their households in Italy. Ann Ist Super Sanità 2004; 40(4):455-461.
104. Gish BA. Interstitial Cystitis/bladder pain syndrome: symptoms, screening and treatment. Nurs Womens Health 2011; 15(6):498-507.
105. Gökyildiz S, Beji NZ. Chronic pelvic pain: gynaecological and non gynaecological causes and consideration for nursing care. Int J of Urol Nurs 2012; 6(1):3-10.
106. Abercrombie PD, Learman LA. Providing holistic care for women with chronic pelvic pain. J Obstet Gynecol Neonatal Nurs 2012; 41(5): 668-679.
107. Collet BJ, Cordle CJ, Steward CR. Setting up a multidisciplinary clinic. Baillieres Best Pract Res Clin Obstet Gynaecol 2000; 14(3):541-556.
108. D’Addio L, Calamandrei C. I Modelli Funzionali della Salute di Marjory Gordon: un’esperienza applicativa nella formazione infermieristica di base. Nursing Oggi 1999; 4: 24-34.
109. O’Leary MP, Sant GR, Fowler FJ Jr, Whitmore KE, Spolarich-Kroll J. The interstitial cystitis symptom index and problem index. Urology. 1997;49(5° suppl):58–63.
110. Heck BN. Interstitial cystitis: enhancing early identification in primary care setting. J Nurse Pract 2007; 3:509-519.
111. Howard FM. Interstitial cystitis: the gynecologist’s guide to diagnosis. OBG Management 2010; 22(7): 33-43.
112. Parson CL, Dell J, Stanford EJ, Bullen M, Kahn BS, Waxell T. et al. Increased prevalence of interstitial cystitis: previously unrecognized urologic and gynecologic cases identified using a new symptom questionnaire and intravescical potassium sensitivity. Urology 2002; 60: 573-578. Heck BN. Intestitial cystitis: enhancing early identification in primary care setting. J Nurse Pract 2007
113. Hanno PM, Burks DA, Clemens JQ, Dmochowski RR, Erickson D, Fitzerald MP et al. AUA Guidelines for the diagnosis and treatment of interstitial cystitis/bladder pain syndrome. J Urol 2011;185(6):2162-70.
114. Howard FM. When treating interstitial cystitis, address all sources of pain. OBJ Management 2010 b; 22(7): 44-49.
115. Shorter B. The potential role of diet in the treatment of interstitial cystitis/painful bladder sindrome. Top Clin Nutr 2006; 21: 312-319.
